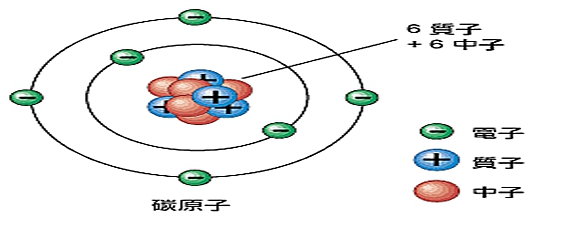
碳原子杂化有:sp杂化,sp2杂化,sp3杂化。
碳原子sp3杂化
碳原子的sp3杂化可以生成4个σ键,形成正四面体构型。例如金刚石、甲烷CH4、四氯化碳CCl4、乙烷C2H6等。
在甲烷分子中,C原子4个sp3杂化轨道与4个H原子生成4个σ共价键,分子构型为正四面体结构。
碳原子sp2杂化
碳原子的sp2杂化生成1个σ键,2个∏键,平面三角形构型。例如石墨、COCl2、C2H4、C6H6等。
在COCl2分子中,C原子以3个sp2杂化轨道分别与2个Cl原子和1个O原子各生成1个σ共价键外,它的未参加杂化的那个p轨道中的未成对的p电子O原子中的对称性相同的1个p轨道上的p电子生成了一个∏共价键,所以在C和O原子之间是共价双键,分子构型为平面三角形。
碳原子sp杂化
生成2个σ键,未杂化轨道生成2个Π键,直线形构型。例如CO2、HCN、C2H2等。
在CO2分子中,C原子以2个sp杂化轨道分别与2个O原子生成2个σ共价键,它的2个未参加杂化的p轨道上的2个p电子分别与2个O原子的对称性相同的2个P轨道上的3个p电子形成2个三中心四电子的大∏键,所以CO2是2个双键。
在HCN分子中,C原子分别与H和N原子各生成1个σ共价键外,还与N原子生成了2个正常的∏共价键,所以在HCN分子中是一个单键,1个叁键。
碳原子sp3杂化
碳原子的sp3杂化可以生成4个σ键,形成正四面体构型。例如金刚石、甲烷CH4、四氯化碳CCl4、乙烷C2H6等。
在甲烷分子中,C原子4个sp3杂化轨道与4个H原子生成4个σ共价键,分子构型为正四面体结构。
碳原子sp2杂化
碳原子的sp2杂化生成1个σ键,2个∏键,平面三角形构型。例如石墨、COCl2、C2H4、C6H6等。
在COCl2分子中,C原子以3个sp2杂化轨道分别与2个Cl原子和1个O原子各生成1个σ共价键外,它的未参加杂化的那个p轨道中的未成对的p电子O原子中的对称性相同的1个p轨道上的p电子生成了一个∏共价键,所以在C和O原子之间是共价双键,分子构型为平面三角形。
碳原子sp杂化
生成2个σ键,未杂化轨道生成2个Π键,直线形构型。例如CO2、HCN、C2H2等。
在CO2分子中,C原子以2个sp杂化轨道分别与2个O原子生成2个σ共价键,它的2个未参加杂化的p轨道上的2个p电子分别与2个O原子的对称性相同的2个P轨道上的3个p电子形成2个三中心四电子的大∏键,所以CO2是2个双键。
在HCN分子中,C原子分别与H和N原子各生成1个σ共价键外,还与N原子生成了2个正常的∏共价键,所以在HCN分子中是一个单键,1个叁键。

爱问教育
2020-04-24 17:21:28